Cho 087 gam hỗn hợp bột các kim loại Fe Al Cu có tỉ lệ mol tương ứng 1 : 2 : 1 vào 400 ml dung dịch

Câu hỏi
Nhận biếtCho 0,87 gam hỗn hợp bột các kim loại Fe, Al, Cu có tỉ lệ mol tương ứng 1 : 2 : 1 vào 400 ml dung dịch (AgNO3 0,08M + Cu(NO3)2 0,5M). Sau khi phản ứng hoàn toàn thì khối lượng chất rắn thu được là (cho Fe = 56, Al = 27, Cu = 64, Ag = 108)
Đáp án đúng: D
Lời giải của Tự Học 365
Giải chi tiết:
Gọi số mol của Fe, Al, Cu lần lượt là x, 2x, x. Ta có:
56x + 27.2x + 64x = 0,87 => x = 0,005 (mol)
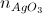 = 0,4.0,08=0,032(mol);
= 0,4.0,08=0,032(mol); 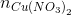 = 0,4.0,5 = 0,2 (mol)
= 0,4.0,5 = 0,2 (mol)
Theo dãy thế điện cực kim loại ta có thứ tự phản ứng:
Al + 3AgNO3 → Al(NO3)3 + 3Ag
0,01 0,03 0,03
AgNO3 còn lại là: 0,032 - 0,03 = 0,002(mol)
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
0,001 0,002 0,002
Fe còn lại là: 0,005 - 0,001 = 0,004(mol)
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
0,004 0,004 0,004
Vậy sau phản ứng chất rắn gồm: 0,032 mol Ag; 0,004 mol Cu và 0,005 mol Cu ban đầu.
=> mchất rắn = 0,032.108 + 0,009.64 = 4,032 (gam) => Chọn D.
Luyện tập
Câu hỏi liên quan
-






Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?




 X
X  Z
Z  T
T  propan-2-ol.
propan-2-ol.