Sục CO2 vào dung dịch Ca(OH)2 và NaOH ta thu được kết quả như hình vẽ.
<

Câu hỏi
Nhận biếtSục CO2 vào dung dịch Ca(OH)2 và NaOH ta thu được kết quả như hình vẽ.

Giá trị của x là:
Đáp án đúng: A
Lời giải của Tự Học 365
Giải chi tiết:
Cách 1: Phân tích phản ứng ở từng đoạn đồ thị
Phản ứng ở các đoạn của đồ thị:
- Đoạn đồ thị đi lên:
(1) CO2 + Ca(OH)2 → CaCO3 + H2O
- Đoạn đồ thị nằm ngang:
(2) CO2 + 2NaOH → Na2CO3 + H2O
(3) CO2 + Na2CO3 + H2O → 2NaHCO3
- Đoạn đồ thị đi xuống:
(4) CO2 + CaCO3 + H2O → Ca(HCO3)2
*Khi nCO2 = a thì (1) kết thúc
⟹ nCO2 = nCaCO3 ⟹ a = 0,1
*Khi nCO2 = a + 0,5 = 0,6 mol thì (3) kết thúc
⟹ Sản phẩm là CaCO3 (0,1 mol) và NaHCO3 (0,6 - 0,1 = 0,5 mol (bảo toàn C))
*Khi nCO2 = x thì đang xảy ra (4)
⟹ Sản phẩm là CaCO3 (0,06 mol); NaHCO3 (0,5 mol); Ca(HCO3)2 (0,1 - 0,06 = 0,04 (bảo toàn Ca))
Bảo toàn C ⟹ nCO2 = nCaCO3 + nNaHCO3 + 2nCa(HCO3)2 = 0,06 + 0,5 + 2.0,04 = 0,64 mol
Cách 2: Sử dụng tính chất của đồ thị
Đồ thị của bài toán cho từ từ CO2 tác dụng với hỗn hợp Ca(OH)2, NaOH có dạng hình thang cân.
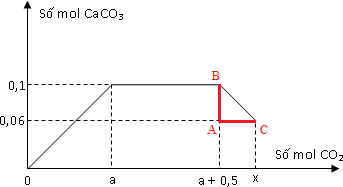
+ Theo đồ thị dễ thấy a = 0,1 mol
+ Quan sát đồ thị ta thấy ABC vuông cân tại A ⟹ AB = AC
⇔ 0,1 - 0,06 = x - (a + 0,5)
Thay a = 0,1 vào ⟹ x = 0,64
Đáp án A
Luyện tập
Câu hỏi liên quan
-

Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là


Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?




