Một bình kín dung tích 1 lít chứa 1,5 mol H2 và 1

Câu hỏi
Nhận biếtMột bình kín dung tích 1 lít chứa 1,5 mol H2 và 1,0 mol N2 (có xúc tác và nhiệt độ thích hợp). Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành. Muốn hiệu suất đạt 25% cần phải thêm vào bình bao nhiêu mol N2?
Đáp án đúng: C
Lời giải của Tự Học 365
Lời giải chi tiết:
Vì thể tích bình 1 lít nên số mol bằng nồng độ mol
N2 + 3H2 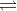 2NH3 (KC)
2NH3 (KC)
Ban đầu 1,0 1,5 0
Cân bằng: 0,9 1,2 0,2
=> KC =  = 0,02572
= 0,02572
Gọi x là số mol N2 cần thêm vào bình để hiệu suất phản ứng đạt 25%. Ta có:
N2 + 3H2 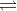 2NH3 (KC)
2NH3 (KC)
Ban đầu: (1,0+x) 1,5 0
Pứ: 0,125 0,375 0,25
Cb: (0,875+x) 1,125 0,25
=>  = 0,02572
= 0,02572
=> x = 0,831 (mol)
=> Đáp án C
Luyện tập
Câu hỏi liên quan
-







Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là


