Ôn đúng trọng tâm – Học chắc từ hôm nay
Hệ thống lại kiến thức lớp 10–11–12
Hòa tan hoàn toàn 1732 gam hỗn hợp X gồm Mg Fe3O4 và Fe(NO3)2 cần vừa đủ dung dịch hỗn hợp gồm 104 m

Câu hỏi
Nhận biếtHòa tan hoàn toàn 17,32 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 cần vừa đủ dung dịch hỗn hợp gồm 1,04 mol HCl và 0,08 mol HNO3 đun nhẹ, thu được dung dịch Y và 2,24 lít hỗn hợp khí Z (đktc) có tỷ khối so với H2 là 10,8 gồm hai khí không màu trong đó có một khí hóa nâu ngoài không khí. Cho dung dịch Y tác dụng với một lượng dung dịch AgNO3 vừa đủ thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng dư dung dịch NaOH, lọc kết tủa nung đến khối lượng không đổi thu được 20,8 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
MZ = 10,8.2 = 21,6 => Z chứa H2
Mà Z chứa 1 khí không màu hóa nâu ngoài không khí nên Z chứa NO
=> Thành phần của Z gồm: NO (a mol) và H2 (b mol)
Giải hệ: nZ = a + b = 0,1 và mZ = 30a + 2b = 0,1.21,6 được a = 0,07 và b = 0,03
Do khí thu được có chứa H2 nên dung dịch Y không chứa NO3-
Sơ đồ hóa bài toán:
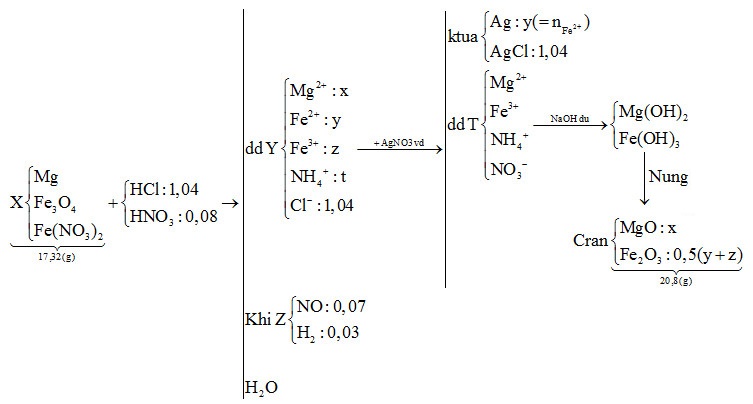
BTNT "H" => nH2O = \(\frac{{{n_{HCl{\text{ }}}} + {\text{ }}{n_{HN{O_3}}}{\text{ }} - {\text{ }}4{n_{N{H_4}^ + }}{\text{ }} - {\text{ }}2{n_{{H_2}}}}}{2}\) = \(\frac{{1,04{\text{ }} + {\text{ }}0,08{\text{ }} - {\text{ }}4t{\text{ }} - {\text{ }}2.0,03}}{2}\) = 0,53 - 2t (mol)
BTNT "N" => nFe(NO3)2 = \(\frac{{{n_{N{H_4}^ + }}{\text{ }} + {\text{ }}{n_{NO}}{\text{ }} - {\text{ }}{n_{HN{O_3}}}}}{2}\) = \(\frac{{t{\text{ }} + {\text{ }}0,07{\text{ }} - {\text{ }}0,08}}{2}\) = 0,5t - 0,005 (mol)
BTNT "Fe" => nFe3O4 = \(\frac{{{n_{F{e^{2 + }}}} + {n_{F{e^{3 + }}}} - {n_{Fe{{(N{O_3})}_2}}}}}{3}\) = \(\frac{{y + z - (0,5t - 0,005)}}{3}\) = \(\frac{{y + z - 0,5t + 0,005}}{3}\) (mol)
+ BTĐT dd Y: 2nMg2+ + 2nFe2+ + 3nFe3+ + nNH4+ = nCl- => 2x + 2y + 3z + t = 1,04 (1)
+ m chất rắn sau nung = mMgO + mFe2O3 => 40x + 160.0,5(y + z) = 20,8 (2)
+ BTKL: mX + mHCl + mHNO3 = m muối + mZ + mH2O
=> 17,32 + 1,04.36,5 + 0,08.63 = 24x + 56y + 56z + 18t + 1,04.35,5 + 0,07.30 + 0,03.2 + 18(0,53 - 2t) (3)
+ mX = mMg + mFe3O4 + mFe(NO3)2 => \(24x + 232.\left( {\frac{{y + z - 0,5t + 0,005}}{3}} \right) + 180.(0,5t - 0,005) = 17,32\) (4)
Giải hệ (1), (2), (3), (4) được x = 0,4; y = 0,01; z = 0,05; t = 0,07
=> m = mAg + mAgCl = 0,01.108 + 1,04.143,5 = 150,32 gam
Đáp án B
Luyện tập
Câu hỏi liên quan
-


Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?







 X
X  Z
Z  T
T  propan-2-ol.
propan-2-ol.