Đốt cháy hoàn toàn 276 gam hỗn hợp X gồm CxHyCOOH CxHyCOOCH3 CH3OH thu được 2688 lít CO2 (đktc) và

Câu hỏi
Nhận biếtĐốt cháy hoàn toàn 2,76 gam hỗn hợp X gồm CxHyCOOH, CxHyCOOCH3, CH3OH thu được 2,688 lít CO2 (đktc) và 1,8 gam H2O. Mặt khác, cho 2,76 gam X phản ứng vừa đủ với 30 ml dung dịch NaOH 1M, thu được 0,96 gam CH3OH. Công thức của CxHyCOOH là
Đáp án đúng: D
Lời giải của Tự Học 365
Giải chi tiết:
Đặt nCxHyCOOH = a ; nCxHyCOOCH3 = b ; nCH3OH = c
nCO2 = 0,12 mol ; nH2O = 0,1 mol
Bảo toàn khối lượng => mO (trong X) = 2,76 - 0,12.12 - 0,1.2 = 1,12 g
=> nO (trong X) = 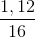 = 0,07 mol => 2a + 2b + c = 0,07
= 0,07 mol => 2a + 2b + c = 0,07
X phản ứng vừa đủ với 0,03 mol NaOH
=> CxHyCOOH và CxHyCOOCH3 phản ứng
=> a + b = 0,03 mol
nCH3OH = 0,03 mol => b +c = 0,03
Giải hệ phương trình: a = 0,01 ; b = 0,02 ; c = 0,01
Đặt CxHy = R
mX = 2,76 => 0,01.(R + 45) + 0,02.(R + 59) + 0,01.32 = 2,76
=> R = 27 (C2H3-)
=> Đáp án D
Luyện tập
Câu hỏi liên quan
-



Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?


Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là


