Cho phản ứng : N2(k) + 3H2(k)
Câu hỏi
Nhận biếtCho phản ứng : N2(k) + 3H2(k) 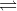 2NH3 (k);
2NH3 (k); 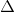 H= -92 kJ. Hai biện pháp đều làm cân bằng chuyển dịch theo chiều thuận là
H= -92 kJ. Hai biện pháp đều làm cân bằng chuyển dịch theo chiều thuận là
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
Tăng áp suất làm cân bằng chuyển dịch theo chiều giảm số mol khí, ở đây là chiều thuận => thỏa mãn
Vì 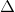 H < 0, phản ứng tỏa nhiệt nên để cân bằng chuyển dịch theo chiều thuận, ta cần hạ nhiệt độ
H < 0, phản ứng tỏa nhiệt nên để cân bằng chuyển dịch theo chiều thuận, ta cần hạ nhiệt độ
=> ý B thỏa mãn
Luyện tập
Câu hỏi liên quan
-




Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là


Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?



