Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm CO2 CO H2 H2O. Dẫn X đi qua 3828 gam hỗn hợp

Câu hỏi
Nhận biếtCho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm CO2, CO, H2, H2O. Dẫn X đi qua 38,28 gam hỗn hợp Fe3O4 và FeCO3 nung nóng thu được hơi nước, 6,72 lít CO2 (đktc) và chất rắn Y gồm Fe, FeO, Fe3O4. Chia Y thành 2 phần bằng nhau:
- Phần 1: Hòa tan hết trong dung dịch chứa a mol HNO3 và 0,0375 mol H2SO4, thu được 3,36 lít (đktc) khí NO là sản phẩm khử duy nhất.
- Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng, thu được dung dịch chứa hai muối có số mol bằng nhau và 5,04 lít khí SO2 (đktc) duy nhất.
Giá trị của a là:
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
Do chia đôi số liệu nên ta lấy một nửa số liệu của 38,28 và 0,3 để phù hợp với việc chia thành 2 phần bằng nhau.
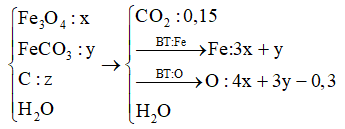
+) mFe3O4 + mFeCO3 = 232x + 116y = 19,14 (1)
+) Bảo toàn C → nCO2 = y + z = 0,15 (2)
+) Xét phản ứng 1/2Y phản ứng với H2SO4 đặc nóng:
Chất rắn Y chứa: Fe (3x + y) và O (4x + 3y - 0,3)
Do nFeSO4 = nFe2(SO4)3 → nFe2+ = (3x + y)/3 và nFe3+ = 2(3x + y)/3
Áp dụng bảo toàn e: 2nFe2+ + 3nFe3+ = 2nO + 2nSO2
\(2.\frac{{3{\rm{x}} + y}}{3} + 3.\frac{{2(3{\rm{x}} + y)}}{3} = 2.(4{\rm{x}} + 3y - 0,3) + 2.0,225\) (3)
Giải (1) (2) (3) được x = 0,06; y = 0,045; z = 0,105
Vậy Y chứa Fe (0,225) và O (0,075).
Giả sử Y với dung dịch hỗn hợp H2SO4, HNO3 tạo Fe2+ (u) và Fe3+ (v)
Bảo toàn Fe → u + v = 0,225 (*)
Bảo toàn electron → 2nFe2+ + 3nFe3+ = 2nO + 3nNO → 2u + 3v = 2.0,075 + 3.0,15 (**)
Giải (*) (**) được u = 0,075 và v = 0,15
Do Y chứa Fe2+ nên NO3- hết hoặc H+ hết
Kiểm tra bảo toàn điện tích dd Y thấy:
Y chứa Fe2+ (0,075); Fe3+ (0,15); SO42- (0,0375) → NO3- (0,525)
Bảo toàn nguyên tố N → nHNO3 = nNO3- + nNO = 0,525 + 0,15 = 0,675 mol
Kết luận a = 0,675
Đáp án B
Luyện tập
Câu hỏi liên quan
-




Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?

Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là



