Cho 2 mol axit axetic tác dụng với 2 mol ancol metylic ( với xúc tác H2SO4 loãng) thấy hiệu suất cự

Câu hỏi
Nhận biếtCho 2 mol axit axetic tác dụng với 2 mol ancol metylic ( với xúc tác H2SO4 loãng) thấy hiệu suất cực đại của quá trình đạt 69,1%. Nếu tiến hành thí nghiệm ở cùng nhiệt độ và xúc tác như trên với 3 mol axit axetic và 4 mol ancol metylic thì hiệu suất cực đại của quá trình este hóa là bao nhiêu?
Đáp án đúng: C
Lời giải của Tự Học 365
Giải chi tiết:
Theo đề bài: CH3COOH + CH3OH 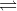 CH3COOCH3 + H2O
CH3COOCH3 + H2O
ban đầu: 2 mol 2 mol
sau phản ứng: 0,618 mol 0,618 mol 1,382 mol 1,382 mol
=> Hằng số cân bằng k = 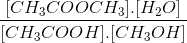 = 5
= 5
Nếu cho 3 mol CH3COOH + 4 mol CH3OH, gọi hiệu suất là h , ta có:
nCH3COOH phản ứng = nCH3OH pứ = 3.h
=> neste = nH2O = 3h
=> nCH3COOH dư = 3 - 3h ; nCH3OH dư = 4 - 3h
=> k = 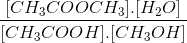 =
= 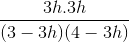 = 5
= 5
Giải ra tìm được h = 0,78 = 78%
=> Đáp án C
Luyện tập
Câu hỏi liên quan
-


Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?







 X
X  Z
Z  T
T  propan-2-ol.
propan-2-ol.