Cho 14 (g) bột Fe tác dụng với 1 lít dung dịch FeCl3 01M và CuCl2 015M. Kết thúc phản ứng thu được c

Câu hỏi
Nhận biếtCho 14 (g) bột Fe tác dụng với 1 lít dung dịch FeCl3 0,1M và CuCl2 0,15M. Kết thúc phản ứng thu được chất rắn A có khối lượng:
Đáp án đúng: C
Lời giải của Tự Học 365
Giải chi tiết:
Ta có: nFe = 14/56 = 0,25 mol
nFeCl3 = 0,1.1 = 0,1 mol
nCuCl2 = 0,15.1 = 0,15 mol
Phản ứng xảy ra theo trình tự :
Fe + 2FeCl3 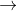 3FeCl2 (1)
3FeCl2 (1)
0,05 0,1 0,15
=> Số mol Fe còn để phản ứng với CuCl2 là: 0,25 – 0,05 = 0,2 mol
Fe + CuCl2 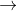 FeCl2 + Cu (2)
FeCl2 + Cu (2)
0,15 0,15 0,15
Theo phản ứng (1), (2) chất rắn A gồm Cu và Fe dư:
0,2 – 0,15 = 0,05 mol
=> mA = mFe dư + mCu = 56.0,05 + 64.0,15 = 12,4 (g)
=> Đáp án C
Luyện tập
Câu hỏi liên quan
-








Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?



 X
X  Z
Z  T
T  propan-2-ol.
propan-2-ol.