Trong một bình kín có cân bằng hóa học sau: 2NO2(k) <

Câu hỏi
Nhận biếtTrong một bình kín có cân bằng hóa học sau: 2NO2(k) 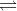 N2O4(k)
N2O4(k)
Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và nhiệt độ T2 bằng 34,5. Biết T1> T2. Phát biểu nào sau đây về cân bằng trên là đúng?
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
2NO 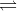 N2O4
N2O4
T1 dhh/H2 = 27,6
T2 dhh/H2 = 34,5
T1 > T2
=> nhiệt độ giảm => tỉ khối tăng => cân bằng chuyển dịch theo chiều thuận
=> Phản ứng thuận tỏa nhiệt.
=> Đáp án B
Luyện tập
Câu hỏi liên quan
-







Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?



 X
X  Z
Z  T
T  propan-2-ol.
propan-2-ol.