(ĐHKB – 2009): Điện phân có màng ngăn 500ml dung dịch chứa hỗn hợp gồm CuCl2 01M và NaCl 05M (điện c

Câu hỏi
Nhận biết(ĐHKB – 2009): Điện phân có màng ngăn 500ml dung dịch chứa hỗn hợp gồm CuCl2 0,1M và NaCl 0,5M (điện cực trơ, hiệu suất điện phân 100%) với cường độ dòng điện 5A trong 3860 giây. Dung dịch thu được sau điện phân có khả năng hòa tan m gam Al. Giá trị lớn nhất của m là
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
Ta có: nCuCl2 = 0,05 mol ; nNaCl = 0,25 mol
=> 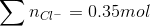
Số mol e trao đổi: 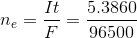 = 0,2 mol
= 0,2 mol
Các bán phản ứng xảy ra ở các điện cực:
Anot (+) : Cl- ; H2O
2Cl- 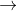 Cl2 + 2e
Cl2 + 2e
0,2 0,2
=> Cl- còn dư; H2O chưa bị oxi hóa
Catot (-): Na+ ; Cu2+ ; H2O
Cu2+ + 2e 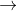 Cu
Cu
0,05 0,1
=> ne trao đổi còn = 0,2 - 0,1 = 0,1 mol
2H2O + 2e 2OH- + H2
Phản ứng hòa tan Al:
Al + OH- + H2O 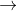 AlO2- +
AlO2- +  H2
H2
0,1 0,1
=> mAl = 27.0,1 = 2,7 g
=> Đáp án B
Luyện tập
Câu hỏi liên quan
-




Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là



Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?



