Oxi hóa chậm m gam Fe ngoài không khí thu được 12 gam hỗn hợp x gồm FeO Fe3O4 Fe2O3 và Fe dư. Hòa ta

Câu hỏi
Nhận biếtOxi hóa chậm m gam Fe ngoài không khí thu được 12 gam hỗn hợp x gồm FeO, Fe3O4, Fe2O3 và Fe dư. Hòa tan X vừa đủ bởi 200ml dung dịch HNO3 thu được 2,24 lít khí NO ( chất khử duy nhất, đo ở đktc). Giá trị của m và nồng độ mol dung dịch HNO3 lần lượt là
Đáp án đúng: D
Lời giải của Tự Học 365
Giải chi tiết:
Sơ đồ các biến đổi xảy ra theo bài toán:
Fe 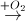 X
X 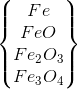
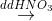 Khí NO(2,24 lít ,đktc)
Khí NO(2,24 lít ,đktc)
↓
Dung dịch Fe(NO3)3
m gam 12 gam
a)Tìm m:
cách 1: sử dụng phương pháp bảo toàn electron
‘-Các quá trình cho nhận electron:
Fe0 → Fe3+ + 3e O20 +4e → 2O2-2
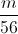 →
→ 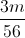
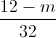 →
→ 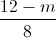
=> 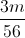 =
= 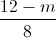 +0,3 => m = 10,08 (gam)
+0,3 => m = 10,08 (gam)
Cách 2: X { FeO, Fe3O4, Fe2O3 và Fe dư } ↔{ Fe: a(mol); O: b(mol)}
=> 56a + 16b = 12 (I)

=> 3a = 2b + 0,3 (II)
Từ (I) và (II) => a = 0,18; b= 0,12 ; m = mFe= 56 x 0,18 = 10,08 ( gam)
b,Tìm nồng độ
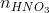 =
= 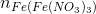 + nN(NO) = 3 x 0,18 + 0,1 = 0,64 (mol)
+ nN(NO) = 3 x 0,18 + 0,1 = 0,64 (mol)
=> [ HNO3] = 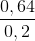 = 3,2 M.
= 3,2 M.
=>Đáp án D.
Luyện tập
Câu hỏi liên quan
-


Cho sơ đồ phản ứng:
H2
 X
X  Y
Y  Z
Z  T
T  propan-2-ol.
propan-2-ol.Biết X, Y, Z, T đều là sản phẩm chính. Công thức cấu tạo thu gọn của X và Z lần lượt là








