Rót từ từ dung dịch HCl vào dung dịch hỗn hợp X chứa a mol K2CO3 và 125a mol KHCO3 ta có đồ thị như

Câu hỏi
Nhận biếtRót từ từ dung dịch HCl vào dung dịch hỗn hợp X chứa a mol K2CO3 và 1,25a mol KHCO3 ta có đồ thị như hình sau:
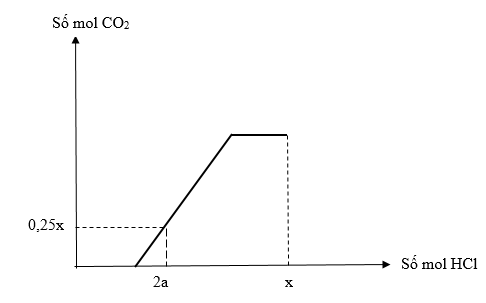
Khi số mol HCl là x thì dung dịch chứa 97,02 gam chất tan. Giá trị của a là
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
+ Khi cho tử từ dd HCl vào hỗn hợp X chứa K2CO3 và KHCO3 xảy ra phản ứng theo thứ tự:
H+ + CO32- → HCO3- (1)
H+ + HCO3- → CO2↑ + H2O (2)
+ Tại nHCl = 2a (mol) thì nCO2 = 0,25x (mol)
Áp dụng công thức ta có:
nCO2 = ∑nH+ - nCO32-
=> 0,25x = 2a – a
=> x = 4a (*)
+ Để pư (1) và (2) xảy ra hoàn toàn cần 1 lượng H+ là: nH+ = nCO32- + nHCO3- bđ + nHCO3(1)
=> nH+ = a + 1,25a + a = 3,25a (mol)
+ Tại nHCl = x (mol) đồ thị đi ngang tức CO2 không thoát ra nữa và dung dịch chứa 97,02 gam chất tan
=> dd chứa: KCl: 3,25a (mol) và HCl dư = x – 2,25a (mol)
=> mchất tan = mKCl + mHCl dư
=> 97,02 = 3,25a.74,5 + (x-3,25a).36,5
=> 123,5a + 36,5x = 97,02 (**)
Từ (*) và (**) a = 0,36 và x = 1,44
Đáp án B
Luyện tập
Câu hỏi liên quan
-






Xét hệ cân bằng hóa học sau xảy ra trong bình kín: C (rắn) + H2O (hơi) <-> CO (khí) + H2 (khí)
Tác động nào sau đây vào hệ (giữ nguyên các điều kiện khác) không làm chuyển dịch cân bằng?



 X
X  Z
Z  T
T  propan-2-ol.
propan-2-ol.
