Ôn đúng trọng tâm – Học chắc từ hôm nay
Hệ thống lại kiến thức lớp 10–11–12
Hòa tan hoàn toàn 12,8 gam hỗn hợp X gồm Mg và Fe vào dung dịch HNO3 l

Câu hỏi
Nhận biếtHòa tan hoàn toàn 12,8 gam hỗn hợp X gồm Mg và Fe vào dung dịch HNO3 lõang vừa đủ. Sau phản ứng thu được dung dịch Y và 6,72 lít khí NO (đktc, là sản phẩm khử duy nhất).
a) Tính % khối lượng mỗi kim loại trong hỗn hợp X. (1,5 đ)
b) Cô cạn dung dịch Y rồi nung đến khối lượng không đổi thu được m gam chất rắn. Tính giá trị của m. (1,0 đ)
c) Trộn ½ lượng hỗn hợp X với bột lưu huỳnh vừa đủ rồi nung nóng đến phản ứng hoàn toàn thu được hỗn hợp Z. Hòa tan hết Z vào dung dịch chứa lượng dư hỗn hợp NaNO3 và HCl. Sau phản ứng thu được V lít khí NO duy nhất. Tính V. (0,5 đ)
(Cho biết: Mg =24 ; Fe=56 ; H=1 ; N=14, O=16, S=32)
Đáp án đúng:
Lời giải của Tự Học 365
Giải chi tiết:
3Mg + 8HNO3 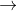 3Mg(NO3)2 + 2NO +4 H2O
3Mg(NO3)2 + 2NO +4 H2O
x x 2/3.x
Fe + 4HNO3 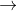 Fe(NO3)3 + NO + 2H2O
Fe(NO3)3 + NO + 2H2O
y x y
n NO = 0,3 mol
gọi x và y lần lượt là số mol của Al và Cu
24x + 56y = 12,8 x = 0,3
x + 2/3.y = 0,3 y = 0,1
% Mg = 56,25%; %Cu = 43,75%
Mg(NO3)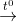 2 MgO + 2NO2 + 1/2O2
2 MgO + 2NO2 + 1/2O2
0,3 0,3
2Fe(NO3)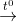 3 Fe2O3 + 6NO2 + 3/2O2
3 Fe2O3 + 6NO2 + 3/2O2
0,1 0,05
m = 20 gam
Phương pháp bảo toàn electron
MgS 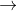 Mg+2 +S+6+ 8e N+5 +3e
Mg+2 +S+6+ 8e N+5 +3e 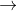 N+2
N+2
0,15 1,2 1,65 0,55
FeS 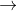 Fe+3 + S+6+ 9e
Fe+3 + S+6+ 9e
0,05 0,45
V=0,55.22,4 =12,32 (lit)
