Hỗn hợp X gồm 4 chất khí sau: CO2; SO3; SO2 và H2. Trình bày phương pháp hóa học nhận biết sự có mặt

Câu hỏi
Nhận biếtHỗn hợp X gồm 4 chất khí sau: CO2; SO3; SO2 và H2. Trình bày phương pháp hóa học nhận biết sự có mặt của các khí trong hỗn hợp X.Viết các phương trình phản ứng xảy ra. Số phản ứng xảy ra là?
Đáp án đúng: C
Lời giải của Tự Học 365
Giải chi tiết:
Lấy một mẫu khí X làm thí nghiệm:
B1: Dẫn hỗn hợp X qua dung dịch BaCl2 dư, nhận ra SO3 và loại bỏ được SO3. Hiện tượng: có BaSO4↓ (màu trắng, không tan trong HCl)
PTHH: SO3 + H2O + BaCl2 → BaSO4↓ + 2HCl
B2: Dẫn hỗn hợp khí sau khi đi ra khỏi bình dd BaCl2 vào dung dịch Br2 dư, nhận ra và loại bỏ khí SO2. Hiện tượng: mất màu nâu đỏ của nước brom.
PTHH: SO2 + H2O + Br2 → H2SO4 + 2HBr
B3: Dẫn hỗn hợp khí sau khi đi ra khỏi bình dung dịch brom, vào dung dịch nước vôi trong dư, nhận ra và loại bỏ CO2. Hiện tượng: dung dịch nước vôi trong hóa đục do có CaCO3↓
PTHH: CO2 + Ca(OH)2 → CaCO3↓ + H2O
B4: Khí còn lại dẫn qua ống đựng CuO nung nóng nhận ra H2. HIện tượng có Cu màu đỏ.
PTHH: H2 + CuO  Cu + H2O
Cu + H2O
Luyện tập
Câu hỏi liên quan
-





Trong phòng thí nghiệm, điều chế các chất khí K,L,M,N,G theo sơ đồ sau:
Cu + H2SO4 đặc → K ↑+ ....
FeS + HCl
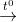 L ↑ +....
L ↑ +....H2O2
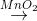 M↑ +....
M↑ +....CaC2 + H2O → N ↑ + ....
Al4C3 + H2O → G ↑ + ...
Số chất khí có thể làm mất màu nước brom là





Có 4 ống nghiệm cùng thể tích, mỗi ống đựng một trong bốn khí sau (không theo thứ tự): O2, H2S, SO2, và HCl. Lật úp từng ống nghiệm và nhúng vào các chậu nước thì kết quả thu được như các hình vẽ dưới đây:
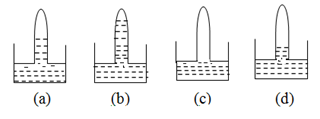
Vậy các bình a, b, c, và d lần lượt chứa các khí

