Cho Cl2 tác dụng với bột Fe thu được muối A. Cho 1625 gam muối A tác dụng với dung dịch AgNO3 dư tạ

Câu hỏi
Nhận biếtCho Cl2 tác dụng với bột Fe thu được muối A. Cho 16,25 gam muối A tác dụng với dung dịch AgNO3 dư tạo ra 43,05 gam kết tủa. Xác định công thức của muối A trên cơ sở các dữ kiện đã cho.
Đáp án đúng: B
Lời giải của Tự Học 365
Giải chi tiết:
Gọi hóa trị của Fe là x
2 Fe + xCl2 2FeClx (1)
FeClx + xAgNO3 xAgCl↓ + Fe(NO3)x (2)
nAgNO3 =\(\frac{{43,05}}{{108 + 14 + 16 \times 3}} = 0,3\)( mol)
Theo (2): \({n_{FeClx}} = {1 \over x}{n_{AgCl}} = {{0,3} \over x}\,mol\)
Ta có: mA= nFeClx . MFeClx
\( = > {\rm{ }}16,25 = {{0,3} \over x}.(56 + 35,5x)\)
=> x = 3
Vậy công thức của muối là FeCl3
Đáp án B
Luyện tập
Câu hỏi liên quan
-









Trong phòng thí nghiệm, điều chế các chất khí K,L,M,N,G theo sơ đồ sau:
Cu + H2SO4 đặc → K ↑+ ....
FeS + HCl
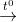 L ↑ +....
L ↑ +....H2O2
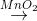 M↑ +....
M↑ +....CaC2 + H2O → N ↑ + ....
Al4C3 + H2O → G ↑ + ...
Số chất khí có thể làm mất màu nước brom là

Có 4 ống nghiệm cùng thể tích, mỗi ống đựng một trong bốn khí sau (không theo thứ tự): O2, H2S, SO2, và HCl. Lật úp từng ống nghiệm và nhúng vào các chậu nước thì kết quả thu được như các hình vẽ dưới đây:
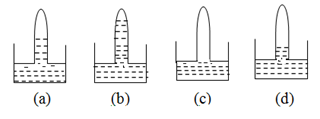
Vậy các bình a, b, c, và d lần lượt chứa các khí

