Khi nhúng thanh Mg có khối lượng m gam vào dung dịch hỗn hợp X chứa a mol Cu(NO3)2 và b mol HCl ta có đồ thị biểu diễn sự phụ thuộc của khối lượng Mg vào thời gian phản ứng được biểu diễn như hình vẽ dưới đây: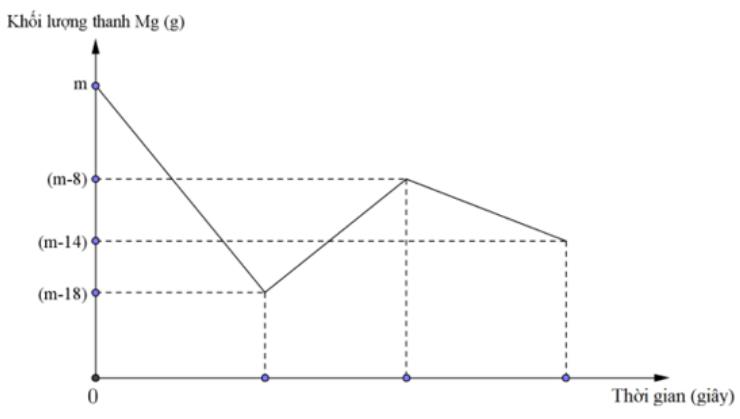
Sau khi phản ứng xảy ra hoàn toàn, rút thanh Mg ra, thu được NO là sản phẩm khử duy nhất của N+5. Tỉ lệ a : b là
Phương pháp giải
Đoạn 1: Khối lượng Mg giảm 18 gam (0,75 mol)
3Mg + 8H+ + 2NO3- → 3Mg2+ + 2NO + 4H2O
=> số mol H+ phản ứng với Mg và NO3- (1)
Đoạn 2: Khối lượng Mg tăng 18 – 8 = 10 gam
+) Sử dụng tăng giảm khối lượng => a
Đoạn 3: Khối lượng Mg giảm 14 – 8 = 6 gam => nMg = 0,25 mol
Mg + 2H+ → Mg2+ + H2
=> số mol H+ phản ứng với Mg tạo H2 (2)
=> b = nH+ (1) + nH+ (2)
=> a : b
Lời giải của Tự Học 365
Đoạn 1: Khối lượng Mg giảm 18 gam (0,75 mol)
3Mg + 8H+ + 2NO3- → 3Mg2+ + 2NO + 4H2O
0,75 → 2
Đoạn 2: Khối lượng Mg tăng 18 – 8 = 10 gam
Mg + Cu2+ → Mg2+ + Cu
a a a
∆m = 64a – 24a = 10 => a = 0,25
Đoạn 3: Khối lượng Mg giảm 14 – 8 = 6 gam => nMg = 0,25 mol
Mg + 2H+ → Mg2+ + H2
0,25 → 0,5
Vậy nH+ = b = 2 + 0,5 = 2,5
=> a : b = 1 : 10
Đáp án cần chọn là: a
Hóa Lớp 12
