Nguyên tố clo có số hiệu nguyên tử là 17. a) Viết cấu hình e của nguy

Câu hỏi
Nhận biếtNguyên tố clo có số hiệu nguyên tử là 17.
a) Viết cấu hình e của nguyên tử clo và xác định vị trí của clo trong bảng tuần hoàn (giải thích).
b) Điền thông tin vào bảng sau:
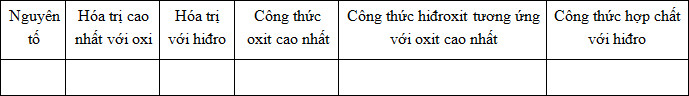
c) Viết công thức electron, công thức cấu tạo phân tử hợp chất của clo với hiđro.
d) Viết phương trình hoá học của phản ứng tạo thành liên kết ion khi Cl2 tác dụng với kim loại K (nhóm IA).
Đáp án đúng:
Lời giải của Tự Học 365
Giải chi tiết:
a) Cấu hình e là 1s22s22p63s23p5
Vị trí: + Ô số 17 vì Z = 17
+ Nhóm VIIA vì là nguyên tố p, nguyên tử có 7 e ở lớp ngoài cùng.
+ Chu kì 3 vì nguyên tử có 3 lớp e.
b) Nguyên tố Cl thuộc nhóm VIIA thì:
+ Hóa trị cao nhất với oxi của Cl là 7
+ Hóa trị trong hợp chất khí với H là 1
Vậy ta có bảng sau:
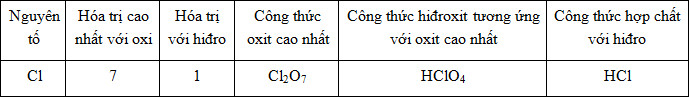
c) Công thức electron và CTCT của HCl:
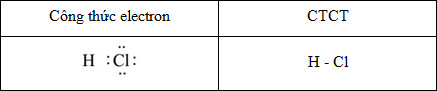
d) Phương trình hoá học của phản ứng tạo thành liên kết ion khi Cl2 tác dụng với kim loại K (nhóm IA):
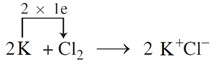
Luyện tập
Câu hỏi liên quan
-





Các nguyên tố thuộc cùng một nhóm A có tính chất hóa học tương tự nhau, vì vỏ nguyên tử của các nguyên tố nhóm A có ?


Một nguyên tố ở chu kì 3, nhóm VIA trong bảng tuần hoàn các nguyên tố hóa học. Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố đó là:


