Hòa tan hoàn toàn hỗn hợp gồm Fe và Zn bằng một lượng vừa đủ dung dịch H2SO4 10% thu được dung dịch

Câu hỏi
Nhận biếtHòa tan hoàn toàn hỗn hợp gồm Fe và Zn bằng một lượng vừa đủ dung dịch H2SO4 10%, thu được dung dịch Y và 22,4 lít H2 (đktc). Nồng độ của ZnSO4 trong dung dịch Y là 11,6022%. Tính khối lượng của mỗi kim loại trong hỗn hợp X?
Đáp án đúng: A
Lời giải của Tự Học 365
Giải chi tiết:
Số mol H2 = 22,4: 22,4 = 1 mol. Goi số mol Fe là x và số mol Zn là y
Fe + H2SO4 → FeSO4 + H2 (1)
Mol x→ x→ x→ x
Zn + H2SO4 → ZnSO4 + H2 (2)
Mol y→ y→ y→ y
=>Số mol H2SO4 = số mol H2 = (x+y) = 1 (*)
Khối lượng dung dịch H2SO4 = 98 . 100/10 = 980 gam
mdd = 56x +65y + 980 – 2 = (56x + 65y +978)
C%(ZnSO4) = 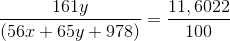
=>15345,857y – 649,7232x = 11346,9516 (**)
Giải hệ PT (*) và (**): x = 0,25; y = 0,75
=>mFe = 0,25.56 = 14g; mZn = 0,75.65 = 48,75g
