Dung dịch A chứa H2SO4 FeSO4 và MSO4; dung dịch B chứa NaOH 05M và BaCl2. Để trung hòa 200ml dung

Câu hỏi
Nhận biếtDung dịch A chứa H2SO4, FeSO4, và MSO4; dung dịch B chứa NaOH 0,5M và BaCl2. Để trung hòa 200ml dung dịch A cần dùng vừa đủ 40ml dung dịch B. Mặt khác khi cho 200ml dung dịch A tác dụng với 300ml dung dịch B thì thu được dung dịch C và 21,07 gam kết tủa D gồm một muối và hai hiđroxit. Để trung hòa dung dịch C cần 40ml dung dịch HCl 0,25 M. Cho biết trong dung dịch C vẫn còn BaCl2 dư. Kim loại M là gì? Biết rằng nguyên tử khối của M lớn hơn nguyên tử khối của Na
Đáp án đúng: C
Lời giải của Tự Học 365
Giải chi tiết:
Phương trình phản ứng
H2SO4 + 2NaOH → Na2SO4 + H2O (1)
0,01 ← 0,02 0,01
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4 (2)
X 2x x x
MSO4 + 2NaOH → M(OH)2 + Na2SO4 (3)
Y 2y y y
4Fe(OH)3 + 2 H2O + O2 → 4Fe(OH)3↓ (4)
x x
Na2SO4 + BaCl2 → BaSO4 ↓ + 2NaCl (5)
(0,01 + x +y) (0,01 + x +y)
D: M(OH)2 ; Fe(OH)3; BaSO4
C: NaOH; BaCl2; NaCl
NaOH + HCl → NaCl + H2O (6)
0,01 0,01
nNaOH ban đầu = 0,15
nNaOH (2), (3) = 0,15 – 0,01 – 0,02 = 0,12 (mol)
x + y = 0,06
Khối lượng trung bình của: M(OH)2; Fe(OH)3 là
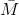 M(OH)2; Fe(OH)3 =
M(OH)2; Fe(OH)3 = 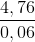 = 79,33
= 79,33
Ta có 23 < M < 45,33
Vậy kim loại phù hợp là Mg
