Đun nóng m gam tinh bột trong dung dịch axit loãng thu đ

Câu hỏi
Nhận biết(1,5 điểm)
Đun nóng m gam tinh bột trong dung dịch axit loãng thu được dung dịch X, Trung hòa lượng axit dư trong dung dịch X rồi chia làm 2 phần :
- Phần 1 : đem thực hiện phản ứng tráng gương hoàn toàn thu được 10,8g Ag
- Phần 2 : đem thực hiện phản ứng lên men rượu, toàn bộ lượng rượu thu được pha chế thành 25 ml rượu 460. Cho kim loại Na(dư) tác dụng với 25ml rượu này thu được V lit khí H2 (dktc).
a. Viết các phương trình hóa học của các phản ứng xảy ra.
b. Tính m và V
( BIết hiệu suất phản ứng thủy phân và phản ứng lên men đều đạt 80%; khối lượng riêng của rượu etylic là 0,8g/ml , khối lượng riêng của nước là 1g/ml)
Đáp án đúng:
Lời giải của Tự Học 365
Giải chi tiết:
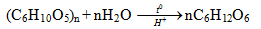
P1 : C6H12O6 + 2[Ag(NH3)2]OH -> C5H11O5COONH4 + 2Ag + 3NH3 + H2O
P2 : C6H12O6 -> 2CO2 + 2C2H5OH
Na + C2H5OH -> C2H5ONa + ½ H2
Na + H2O -> NaOH + ½ H2
b.
Phần 1 : nC6H12O6(1) = 1/2nAg = 0,05 mol
Phần 2 : Trong 25 ml rượu 460 có : VC2H5OH = 11,5 ml ; VH2O = 13,5 ml
=> mC2H5OH = 11,5.0,8 = 9,2g ; mH2O = 13,5g
=> nC2H5OH = 0,2 mol ; nH2O = 0,75 mol
=> nH2 = ½ (nC2H5OH + nH2O) = 0,475 mol => VH2(dktc) = 10,64 lit
=> nC6H12O6(2) = ½ nC2H5OH : H% = ½.0,2.100/80 = 0,125 mol
Cò : nC6H12O6 bđ = 0,175 mol
=> ntinh bột ban đầu = nC6H12O6 bđ /(n.H%) = 0,175/(n.80%) = 0,21875/n (mol)
=> m = 35,4375g
