Đốt cháy hoàn toàn 01 mol hỗn hợp X gồm CH4 C2H4 và C2H6 sản phẩm thu được dẫn qua bình 1 đựng H2SO4

Câu hỏi
Nhận biếtĐốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm CH4, C2H4 và C2H6 sản phẩm thu được dẫn qua bình 1 đựng H2SO4 đặc và bình 2 đựng dung dịch Ca(OH)2 dư. Sau thí nghiệm thấy bình 2 có 15 gam kết tủa và khối lượng bình 2 tăng nhiều hơn bình 1 là 2,55 gam. thành phần % về thể tích của mỗi khí trong X lần lượt là
Đáp án đúng: C
Lời giải của Tự Học 365
Giải chi tiết:
nCaCO3 = 15/100= 0,15 mol
CO2 + Ca(OH)2 → CaCO3 + H2O
0,15 0,15
nCO2 = 0,15 mol
m bình 2 hơn bình 1 = mCO2 - mH2O = 2,55
=> 0,15.44 - mH2O = 2,55
=> mH2O = 4,05 gam
=> nH2O= 0,225 mol
gọi công thức chung của hỗn hợp ban đầu là \({C_{\overline x }}{H_{\overline y }}\)
\(\begin{gathered}
{C_{\overline x }}{H_{\overline y }} \to \overline x C{O_2} + \frac{{\overline y }}{2}{H_2}O \hfill \\
0,1\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,1\overline x \,\,\,\,\,\,\,\,\,\,\,\,\,0,05\overline y \hfill \\
\left\{ \begin{gathered}
0,1\overline x = 0,15 \to \overline x = 1,5 \hfill \\
0,05\overline y = 0,225 \to \overline y = 4,5 \hfill \\
\end{gathered} \right. \hfill \\
\hfill \\
\end{gathered} \)
* \(\overline x = 1,5\)
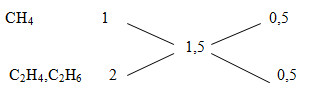
=> %CH4 =50%
* \(\overline y = 4,5\)
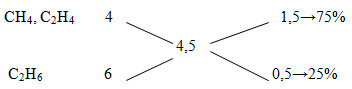
=> % C2H6 = 25%
=> % C2H4 = 100%-25%-50% = 25%
Đáp án C
