Chia 16 gam một oxit kim loại MO thành 2 phần bằng nhau: Phần 1: Hòa tan trong dung dịch HCl dư làm

Câu hỏi
Nhận biếtChia 16 gam một oxit kim loại MO thành 2 phần bằng nhau:
Phần 1: Hòa tan trong dung dịch HCl dư, làm bay hơi cẩn thận dung dịch sau phản ứng thu được 17,1 gam một muối clorua X
Phần 2: Cho tác dụng với dung dịch H2SO4 loãng dư, làm bay hơi cẩn thận dung dịch sau phản ứng thu được 25,0 gam một muối sunfat Y
Xác định M và công thức hai muối X, Y. (Biết MX < 180 gam/mol, MY < 260 gam/mol)
Đáp án đúng: A
Lời giải của Tự Học 365
Giải chi tiết:
Các PTHH:
MO + 2HCl → MCl2 + H2O (1)
MO + H2SO4 → MSO4 + H2O (2)
Ta có: Nếu muối clorua là MCl2, theo (1) và giả thiết ta có:
 => 8(M + 71) = 17,1(M + 16) => M = 32,35
=> 8(M + 71) = 17,1(M + 16) => M = 32,35
Không có kim loại M hóa trị II và NTK = 32,5 => Loại
Vậy điều này chứng tỏ các muối đó là những muối ngậm nước
Gọi công thức các muối ngậm nước lần lượt như sau:
X là MCl2.aH2O và Y là MSO4.bH2O
Xét PƯ (1) ta có: 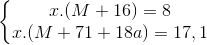 => x =
=> x =  (*)
(*)
Xét PƯ (2) ta có:  => x =
=> x =  (**)
(**)
Từ (*) và (**) suy ra: 91b – 170a = 115 (***)
Do: MX = M + 71 + 18a < 180 => a <  = 6,05
= 6,05
MX = M + 96 + 18b < 250 => a < 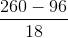 = 9,1
= 9,1
Kết hợp (***) và a, b là số nguyên, b phải chia hết cho 5
Nghiệm thỏa mãn là: b = 5; a = 2; x = 0,1. Suy ra: MX = 64 (Cu)
Vậy công thức muối là: X là CuCl2.2H2O và Y là CuSO4.5H2O
=> Đáp án A
