: (2,0 điểm) 1. (1,0 điểm) Khử hoàn toàn 4,06g một oxit kim loại bằ

Câu hỏi
Nhận biếtBài 4(VD) : (2,0 điểm)
1. (1,0 điểm) Khử hoàn toàn 4,06g một oxit kim loại bằng CO dư ở nhiệt độ cao thu được a gam kim loại M. Khí sinh ra được hấp thụ hết vào bình đựng dung dịch Ca(OH)2, thu được 4,50g kết tủa, đồng thời thấy khối lượng dung dịch giảm 1,42g. Lấy a gam M hòa tan hết vào dung dịch HCl dư thu được 1,176 lit khí H2 (dktc). Cho các phản ứng xảy ra hoàn toàn. Xác định công thức oxit kim loại.
2. (1,0 điểm) Đốt cháy hoàn toàn 3,6g hợp chất hữu cơ X (chứa C, H, O). Dẫn toàn bộ sản phẩm cháy đi qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 7,44g đồng thời thu được 12,0g kết tủa. Cho các phản ứng xảy ra hoàn toàn.
a. Xác định công thức phân tử của X. Biết tỷ khối hơi của X so với oxi là 2,8125.
b. Xác định công thức cấu tạo của X biết :
- 0,1 mol X tác dụng với vừa đủ 100 ml dung dịch NaOH 1M
- 0,1 mol X tác dụng với Na dư thu được 2,24 lit khí H2 (dktc)
Đáp án đúng:
Lời giải của Tự Học 365
Giải chi tiết:
1.
Ta có : Oxit kim loại bị khử tạo khí CO2 hấp thụ vào bình Ca(OH)2 tạo kết tủa CaCO3
Vậy mdung dịch giảm = mCaCO3 – mCO2
=> mCO2 = 4,5 – 1,42 = 3,08g => nCO2 = 0,07 mol
Phương trình khử oxit kim loại tổng quát : MxOy + yCO 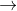 xM + yCO2
xM + yCO2
=> nCO = nCO2 = nO(oxit)
=> mM = moxit – mO(oxit) = 4,06 – 0,07.16 = 2,94g
Khi M + HCl : nH2 = 0,0525 mol
M + nHCl 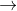 MCln + 0,5nH2
MCln + 0,5nH2
(g) M 0,5n.2
(g) 2,94 0,0525.2
=> M.0,0525.2 = 2,94.0,5n.2
=> M = 28n
=> Vậy n = 2 thì M = 56g (Fe) => nFe = 0,0525
Xét oxit kim loại ban đầu có : nFe : nO = 0,0525 : 0,07 = 3 : 4
Vậy oxit ban đầu có công thức là Fe3O4
2.
a) Đốt cháy X thu được sản phẩm gồm CO2 và H2O cho vào bình Ca(OH)2 dư => cả 2 chất đều bị giữ lại trong bình
nCaCO3 = 0,12 mol
Ca(OH)2 + CO2 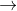 CaCO3 + H2O
CaCO3 + H2O
Mol 0,12 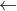 0,12
0,12
mbình tăng = mCO2 + mH2O => mH2O = 7,44 – 44.0,12 = 2,16g
=> nH2O = 0,12 mol
Áp dụng định luật bảo toàn nguyên tố :
nC = nCO2 = nC(X) = 0,12 mol ; nH = nH(X) = 2nH2O = 0,24 mol
Có : mX = mC + mH + mO => mO = 3,6 – 0,12.12 – 0,24.1 = 1,92g
=> nO = 0,12 mol
=> nC : nH : nO = 0,12 : 0,24 : 0,12 = 1 : 2 : 1
=> CTTQ của X là (CH2O)n
Lại có : dX/O2 = 2,8125 => MX = 32.2,8125 = 90g = 30n
=> n = 3 => X là C3H6O3
b) – 0,1 mol X tác dụng với vừa đủ 0,1 mol NaOH => tỉ lệ mol 1 : 1
=> X có nhóm COO
- 0,1 mol X tác dụng với Na dư thu được 0,1 mol H2
=> X có 2 Hidro linh động (-OH , -COOH)
Vậy kết hợp lại X sẽ có 1 nhóm OH và 1 nhóm COOH
Công thức cấu tạo của X là : HO – C2H4 – COOH
