1. Tiến hành thí nghiệm như hình bên: cho kẽm viên vào dung dịch HCl t
Câu hỏi
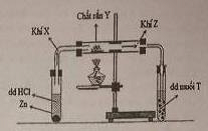
Nhận biết1. Tiến hành thí nghiệm như hình bên: cho kẽm viên vào dung dịch HCl thấy có khí X thoát ra; dẫn khí X đi qua chất rắn Y nung nóng thu được khí Z; sục khí Z vào dung dịch muối T thấy xuất hiện kết tủa màu đen.

Biết rằng: Y là đơn chất rắn, màu vàng, dung dịch muối T có màu xanh và T có khối lượng mol là 160 gam. Xác định các chất X, Y, Z, T. Viết các phương trình hóa học xảy ra.
2. Muối ăn NaCl bị lẫn các tạp chất: Na2SO4, MgCl2, MgSO4, CaCl2, CaSO4. Trình bày phương pháp hóa học loại bỏ các tạp chất để thu được NaCl tinh khiết. Viết các phương trình hóa học xảy ra.
Đáp án đúng:
Lời giải của Tự Học 365
Giải chi tiết:
1.
Y là đơn chất màu vàng: S
T màu xanh và MT = 160 : CuSO4
Khí Z tạo kết tủa đen với CuSO4 nên Z : H2S → X : H2
Zn + 2HCl → ZnCl2 + H2↑
H2 + S \(\xrightarrow{{{t^0}}}\) H2S
H2S + CuSO4 → CuS↓ + H2SO4
2. Cho hỗn hợp qua dung dịch Na2CO3: ion Mg, Ca bị giữ lại dạng kết tủa, lọc bỏ.
MgCl2 + Na2CO3 → MgCO3↓ + 2NaCl
MgSO4 + Na2CO3 → MgCO3↓ + Na2SO4
CaCl2 + Na2CO3 → CaCO3↓ + 2NaCl
CaSO4 ít tan hoặc tan 1 phần tạo kết tủa cũng sẽ được lọc bỏ.
Dung dịch còn lại gồm : NaCl và Na2SO4. Ta cho vào dung dịch BaCl2
Na2SO4 + BaCl2 → BaSO4 + 2NaCl

