Tính lượng chất trong phản ứng polime hóa (cách giải & bài tập có đáp án)

Tính lượng chất trong phản ứng polime hóa (cách giải & bài tập có đáp án)
Bài tập tính lượng chất, hiệu suất trong phản ứng polime hóa
| Bài 1: Khi trùng ngưng axit ε-aminocaproic ta thu được m gam polime và 1,35 gam H2O. Giá trị của m là
A. 8,475. B. 9,825. C. 16,95. D. 5,425. |
Lời giải chi tiết
Axit ε-aminocaproic có CT là H2N(CH2)5COOH
nH2N(CH2)5COOH → [-HN-(CH2)5-CO-]n + nH2O (1)
Theo (1) $\Rightarrow {{n}_{\varepsilon -a\min \text{o}c\text{a}proic}}={{n}_{{{H}_{2}}O}}=\frac{1,35}{18}=0,075\left( mol \right)$
BTKL 131.0,075 = mpolime + 1,35 ⇒ mpolime = 8,475 gam
⇒ Đáp án A
| Bài 2: Xelulozơ trinitrat được điều chế từ xenlulozo và axit nitric đặc có xúc tác axit sunfuric đặc, nóng. Để có 29,7 kg xenlulozo trinitrat, cần dùng dung dịch chứa m kg axit nitric (hiệu suất phản ứng đạt 90 ). Giá trị của m là
A. 42. B. 10. C. 30. D. 21. |
Lời giải chi tiết
[C6H7O2(OH)3]n + 3nHNO3 → [C6H7O2(NO3)3]n + 3nH2O (1)
Theo (1) nxenlulozo trinitrat = 29,7 : 297 = 0,1(kmol)
$\Rightarrow {{n}_{HN{{O}_{3}}}}$phản ứng = 0,1.3 = 0,3 (kmol)
$\Rightarrow {{n}_{HN{{O}_{3}}}}$ban = $0,3.\frac{100}{90}=\frac{1}{3}\left( kmol \right)$
⇒ Đáp án D
| Bài 3: Cho sơ đồ chuyển hóa: CH4 → C2H2 → C2H3Cl → PVC.
Để tổng hợp 250kg PVC theo sơ đồ trên thì cần V m3 khí thiên nhiên (ở đktc). Giá trị của V là (biết CH4 chiếm 80 thể tích khí thiên nhiên và hiệu suất của cả quá trình là 50%) A. 358,4. B. 448,0. C. 286,7. D. 224,0. |
Lời giải chi tiết
Sơ đồ phản ứng:
2CH4 → C2H2 → C2H3Cl → (-CH2-CHCl-)n (1)
Theo (1) $\Rightarrow {{n}_{C{{H}_{4}}}}$phản ứng = 2nPVC $\Rightarrow {{n}_{C{{H}_{4}}}}$phản ứng = $2.\frac{250}{65,5}=8\left( kmol \right)$
$\Rightarrow {{n}_{C{{H}_{4}}}}$ban đầu = $8.\frac{100}{50}=16\left( kmol \right)$
$\Rightarrow V=16.22,4.\frac{100}{80}=448\left( {{m}^{3}} \right)$
⇒ Đáp án B
| Bài 4: Poli (vinyl clorua) (PVC) được điều chế từ khí thiên nhiên (metan chiếm 97% khí thiên nhiên) theo sơ đồ chuyển hóa và hiệu suất mỗi giai đoạn như sau:
Metan $\xrightarrow{15\%}$ Axetilen $\xrightarrow{85\%}$ Vinyl clorua $\xrightarrow{80\%}$ PVC. Muốn tổng hợp 1,0 tấn PVC thì cần bao nhiêu m3 khí thiên nhiên (ở đktc) A. 7245 m3. B. 7,245 m3. C. 3622 m3. D. 3,622 m3. |
Lời giải chi tiết
2CH4 → C2H2 → C2H3Cl → (-CH2-CHCl-)n (1)
Theo (1) $\Rightarrow {{n}_{C{{H}_{4}}}}$ban đầu = $2.\frac{1,0.1000}{62,5}.\frac{100}{80}.\frac{100}{85}.\frac{100}{15}=313,73\left( kmol \right)$
⇒ Thể tích khí thiên nhiên là $313.22,4.\frac{100}{97}=7245\left( {{m}^{3}} \right)$
⇒ Đáp án A
| Bài 5: Thủy phân 500 gam poli(metyl metacrylat) –PMM trong dung dịch H2SO4 loãng, đun nóng. Sau một thời gian thấy tổng khối lượng polime thu được là 454 gam. Hiệu suất phản ứng thủy phân PMM là
A. 80%. B. 65,71%. C. 9,2%. D. 90,8%. |
Lời giải chi tiết
Công thức của PMM là 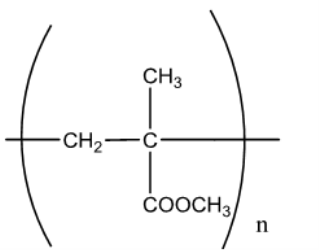
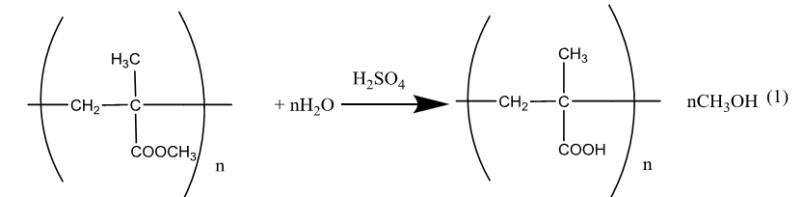
BTKL 500 + 18.x = 454 + 32x ⇒ x = 46/14 (mol)
$\Rightarrow H=\frac{\frac{46}{14}.100}{500}.100=65,71/\%$
⇒ Đáp án B
| Bài 7: Thực hiện phản ứng trùng hợp 25 gam vinyl clorua thu được hỗn hợp. Lượng hỗn hợp này có khả năng làm mất màu 80ml dung dịch brom 1,0M. Hiệu suất phản ứng trùng hợp là
A. 80%. B. 65%. C. 50%. D. 20%. |
Lời giải chi tiết
nCH2=CH-Cl → (-CH2-CH(Cl)-)n (1)
Do hỗn hợp sau phản ứng phản ứng với Br2 ⇒ vinyl clorua dư
CH2=CHCl + Br2 → CH2Br-CHCl(Br) (2)
Theo (2) ⇒ ${{n}_{C{{H}_{2}}=CHCl}}$dư = 0,08(mol)
$\Rightarrow H=\frac{25-62,5.0,08}{25}.100=80\%$
⇒ Đáp án A
| Bài 8: Cho 2,24 lít khí C2H2 (đktc) tác dụng hết với HCl (t0, HgCl2) để điều chế ra vinyl clorua. Sau đó tiến hành phản ứng trùng hợp vinyl clorua thành poli vinyl clorua. Tính khối lượng poli (vinyl clorua) thu được nếu hiệu suất của mỗi quá trình là 90%
A. 5,0625 gam. B. 5,625gam. C. 6,2500 gam. D. 10,1250 gam. |
Lời giải chi tiết
${{n}_{{{C}_{2}}{{H}_{2}}}}=\frac{2,24}{22,4}=0,1\left( mol \right)$
$CH\equiv CH-\to C{{H}_{2}}=CHCl-\to {{\left( -C{{H}_{2}}-CHCl- \right)}_{n}}$
Theo sơ đồ ⇒ nvinyl clorua = 0,1.0,9.0,9 = 0,081(mol)
⇒ mpoli (vinyl clorua) = 62,5.0,081 = 5,0625 gam
⇒ Đáp án A
| Bài 9: Đem trùng hợp 10 mol vinyl axetat, thu được 688 gam poli (vinyl axetat). Hiệu suất quá trình trùng hợp là
A. 100%. B. 90%. C. 80%. D. 70%. |
Lời giải chi tiết
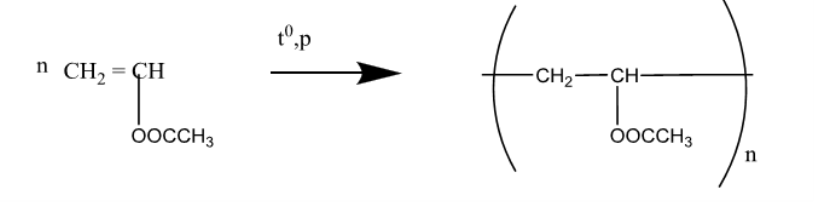
⇒ nvinyl axetat phản ứng = nPVA = 688 : 86 = 8(mol)
$\Rightarrow H=\frac{8}{10}.100=80\%$
⇒ Đáp án C
| Bài 10: Tiến hành tổng hợp PVC bằng cách đun nóng 37,5 gam vinyl clorua với một lượng nhỏ (0,3 – 0,7 ) chất xúc tác benzoyl peoxit. Cho toàn bộ hỗn hợp sau phản ứng (đã loại hết xúc tác) vào 2,0 lít dung dịch Br2 0,1M; sau đó cho thêm KI dư thấy tạo thành 20,32 gam I2. Hiệu suất tổng hợp PVC là
A. 66,7%. B. 80,0%. C. 86,7%. D. 93,3%. |
Lời giải chi tiết
Các phản ứng xảy ra gồm:
nCH2=CH-Cl → (-CH2-CHCl-)n (1)
CH2=CHCl + Br2 → CH2Br-CHCl(Br) (2)
Br2 + 2KI → 2KBr + I2 (3)
Theo (3) $\Rightarrow {{n}_{B{{r}_{2}}\left( 3 \right)}}={{n}_{{{I}_{2}}}}=\frac{20,32}{254}=0,08\left( mol \right)$
$\Rightarrow {{n}_{B{{r}_{2}}\left( 2 \right)}}=0,2-0,08=0,12\left( mol \right)$
$\Rightarrow {{n}_{C{{H}_{2}}=CHCl\left( 2 \right)}}=0,12\left( mol \right)$
$\Rightarrow H=\frac{37,5-0,12.62,5}{37,5}.100=80\%$
⇒ Đáp án B
| Bài 12: Poli stiren (PS) là một polime dạng rắn, màu trắng, không dẫn điện và không dẫn nhiệt. PS được tạo thành từ phản ứng trùng hợp stiren. Khi trùng hợp 10 mol stiren với hiệu suất 80% thì khối lượng P thu được là
A. 650 gam. B. 832 gam. C. 798 gam. D. 900 gam. |
Lời giải chi tiết
nC6H5-CH=CH2 → (-CH2-CH(C6H5)-)n
$\Rightarrow {{n}_{PS}}=0,8.10=8\left( mol \right)\Rightarrow {{m}_{PS}}=104.8=832\left( gam \right)$
⇒ Đáp án B
| Bài 13: Đốt cháy hoàn toàn m gam cao su buna rồi cho toàn bộ sản phẩm cháy đi chậm qua bình đựng dung dịch Ca(OH)2 dư, dung dịch thu được sau phản ứng giảm 25,5 gam so với dung dịch Ca(OH)2 ban đầu. Giá trị của m là
A. 8,10. B. 6,147. C. 3, 98. D. 4,05. |
Lời giải chi tiết
Cao su bu na có CT (C4H6)n
(C4H6)n + O2 → 4nCO2 + 3nH2O
Đặt số mol CO2 : 4x mol ; H2O : 3x mol
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
4x 4x mol
$\Rightarrow 100.4x-44.4x-18.3x=25,5\Rightarrow x=0,15\left( mol \right)$
$\Rightarrow m=54.0,15=8,1\left( gam \right)$
⇒ Đáp án A
| Bài 14: Đốt cháy hoàn toàn một lượng poli etilen (nhựa PE) , sản phẩm cháy lần lượt cho qua bình (1) đựng H2SO4 đặc và bình (2) đựng 2 lít dung dịch Ba(OH)2 0,65M, sau phản ứng thấy khối lượng bình (1) tăng m gam và bình (2) thu được 197 gam kết tủA. Giá trị lớn nhất của m là
A. 18. B. 12. C. 28,8. D. 23,4. |
Lời giải chi tiết
$\Rightarrow {{n}_{Ba{{\left( OH \right)}_{2}}}}=2.0,65=1,3\left( mol \right);{{n}_{BaC{{O}_{3}}}}=197:197=1\left( mol \right)$
Do m lớn nhất nên có các phản ứng sau
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
Mol 1 1 1
2CO2 + Ba(OH)2 → Ba(HCO3)2
Mol 0,6 0,3
$\Rightarrow {{n}_{C{{O}_{2}}}}=1,6\left( mol \right)$
PE có CT (-CH2-CH2-)n
$\Rightarrow {{n}_{{{H}_{2}}O}}=1,6\left( mol \right)\Rightarrow m=1,6.18=28,8\left( gam \right)$
⇒ Đáp án C
| Bài 15: Đốt cháy hoàn toàn một lượng poli propilen rồi dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch nước vôi trong dư thu được 6 gam kết tủa thì khối lượng dung dịch
A. giảm 2,28 gam. B. giảm 3,36 gam. C. giảm 6,0 gam. D. tăng 3,72 gam. |
Lời giải chi tiết
Đốt cháy (C3H6)n $\Rightarrow {{n}_{C{{O}_{2}}}}={{n}_{{{H}_{2}}O}}$
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Theo (1) $\Rightarrow {{n}_{C{{O}_{2}}}}={{n}_{{{H}_{2}}O}}={{n}_{CaC{{O}_{3}}}}=\frac{6}{100}=0,06\left( mol \right)$
${{m}_{C{{O}_{2}}}}+{{m}_{{{H}_{2}}O}}=44.0,06+18.0,06=3,72\left( gam \right)$
mdung dịch giảm = 6 – 3,72 = 2,28 gam
⇒ Đáp án A
| Bài 16: Để điều chế 100 gam thủy tinh hữu cơ cần bao nhiêu gam ancol metylic và bao nhiêu gam axit metacrylic, biết hiệu suất quá trình đạt 80 .
A. 68,8 gam axit và 25,6 gam ancol. B. 86,0 gam axit và 32 gam ancol. C. 107,5 gam axit và 40 gam ancol. D. 107,5 gam axit và 32 gam ancol. |
Lời giải chi tiết
CH2=C(CH3)COOH + CH3OH → CH2=C(CH3)COOCH3 + H2O (1)
CH2=C(CH3)COOCH3 → thủy tinh hữu cơ (2)
Theo (1), (2) $\Rightarrow {{n}_{C{{H}_{3}}OH}}=\frac{100}{100}.\frac{100}{80}=1,25\left( mol \right)\Rightarrow {{m}_{C{{H}_{3}}OH}}=32.1,25=40\left( gam \right)$
⇒ n axit metacrylic = 86.1,25 = 107,5 gam
⇒ Đáp án C
| Bài 17: PVC được điều chế từ khí thiên nhiên theo sơ đồ:
CH4 → C2H2 → CH2=CHCl → PVC Nếu hiệu suất toàn bộ quá trình điều chế là 20% thì thể tích khí thiên nhiên chứa 97% metan (ở đktc) tối thiểu cần lấy để chế ra 1 tấn PVC là A. 1,792 m3. B. 3476 m3. C. 3584 m3. D. 3695 m3. |
Lời giải chi tiết
Sơ đồ phản ứng 2CH4 → C2H2 → CH2=CHCl → PVC
Theo sơ đồ $\Rightarrow {{n}_{C{{H}_{4}}}}=2.\frac{1}{62,5}{{.10}^{3}}.\frac{100}{20}=160\left( kmol \right)$
⇒ Vkhí thiên nhiên = $160.22,4.\frac{100}{97}=3695\left( {{m}^{3}} \right)$
⇒ Đáp án D
| Bài 18: Thủy tinh hữu cơ poli(metyl metacylat) được tổng hợp theo sơ đồ chuyển hóa và hiệu suất mỗi giai đoạn như sau:
Axit metacylic $\xrightarrow{75\%}$ Metyl metacrylat $\xrightarrow{85\%}$ Poli(metyl metarylat) Muốn tổng hợp 1,0 tấn thủy tinh hữu cơ thì cần dùng bao nhiêu tấn axit metacrylic 80% A. 1,349 tấn. B. 1,686 tấn. C. 1,433 tấn. D. 1,265 tấn. |
Lời giải chi tiết
Theo sơ đồ Þ maxit metacrylic = $86.\frac{1}{100}.\frac{100}{85}.\frac{100}{75}=1,349$(tấn)
Þ Khối lượng dung dịch axit metacrylic cần dùng là $1,349.\frac{100}{80}=1,686$ (tấn)
Þ Đáp án B
| Bài 19: Từ 2 mol etanol điều chế thành etilen (t0>1700C, H2SO4 đặc) sau đó tiến hành phản ứng trùng hợp điều chế polietilen với hiệu suất mỗi giai đoạn phản ứng bằng 85% . Khối lượng polietilen thu được là
A. 47,6 gam. B. 40,46 gam. C. 77,51 gam. D. 65,88 gam. |
Lời giải chi tiết
CH3CH2OH $\xrightarrow{{{H}_{2}}S{{O}_{4}},{{170}^{0}}C}C{{H}_{2}}=C{{H}_{2}}-\to {{\left( -C{{H}_{2}}-C{{H}_{2}}- \right)}_{n}}\ \ \left( 1 \right)$
Theo (1) $\Rightarrow {{n}_{polietilen}}=2.0,85.0,85=1,44\left( mol \right)$
Þ mpoli etilen = 28.1,445 = 40,46(gam)
Þ Đáp án B
| Bài 20: Từ tinh bột có thể điều chế cao su buna theo sơ đồ và hiệu suất mỗi giai đoạn như sau: Tinh bột $\xrightarrow{90\%}$ Glucozơ $\xrightarrow{75\%}$ Etanol $\xrightarrow{75\%}$ Buta-1,3-đien $\xrightarrow{80\%}$ poli(buta-1,3-đien)
Khi sử dụng 24,3 tấn tinh bột thì khối lượng cao su buna điều chế được là bao nhiêu (giả thiết cao su buna gồm 70% poli buta -1,3-đien) A. 3280,5 kg. B. 4686,4 kg. C. 2296,35 kg. D. 8100 kg. |
Lời giải chi tiết
Sơ đồ phản ứng:
(C6H10O5)n $\xrightarrow{90\%}$ C6H12O6 $\xrightarrow{75\%}$ 2C2H5OH $\xrightarrow{75\%}$ CH2=CH-CH=CH2 $\xrightarrow{80\%}$ poli buta -1,3-đien
Theo sơ đồ ta có $\Rightarrow {{m}_{polibutadien}}=\frac{24,3}{162}.\frac{90}{100}.\frac{75}{100}.\frac{75}{100}.\frac{80}{100}.54.\frac{100}{70}=4,686$
Þ Đáp án B
| Bài 21: Cao su buna được sản xuất từ gỗ chứa 50% xenlulozo theo sơ đồ:
Xenlulozo $\xrightarrow{\left( 1 \right)}$ Glucozo $\xrightarrow{\left( 2 \right)}$ Etanol $\xrightarrow{\left( 3 \right)}$ buta – 1,3 – đien $\xrightarrow{\left( 4 \right)}$ cao su buna Hiệu suất của 4 giai đoạn lần lượt là 60% , 80% , 75% và 100% . Để sản xuất 1,0 tấn cao su buna cần bao nhiêu tấn gỗ A. 8,33. B. 16,2. C. 8,1. D. 16,67. |
Lời giải chi tiết
Sơ đồ phản ứng:
(C6H10O5)n $\xrightarrow{60\%}$ C6H12O6 $\xrightarrow{80\%}$ 2C2H5OH $\xrightarrow{75\%}$ CH2=CH-CH=CH2 $\xrightarrow{100\%}$ poli buta -1,3-đien
Theo sơ đồ phản ứng $\Rightarrow {{m}_{Xenlulozo}}=162.\frac{1}{54}.\frac{100}{75}.\frac{100}{80}.\frac{100}{60}=8,333$ (tấn)
Þ mgỗ = $8,333.\frac{100}{50}=16,67$ (tấn)
Þ Đáp án D
| Bài 22: Từ ancol etylic, sau khi điều chế buta-1,3-đien, người ta trùng hợp buta-1,3-đien thành cao su buna với hiệu suất của cả quá trình là 80%. Để điều chế được 27kg cao su buna thì khối lượng C2H5OH tối thiểu cần dùng là
A. 57,5 kg. B. 46,0 kg. C. 36,8 kg. D. 55,7 kg. |
Lời giải chi tiết
Ta có sơ đồ phản ứng 2C2H5OH → CH2 = CH – CH = CH2 → poli buta-1,3-đien
Theo sơ đồ $\Rightarrow {{m}_{{{C}_{2}}{{H}_{5}}OH}}=46.2.\frac{27}{54}.\frac{100}{80}=57,5\left( kg \right)$
Þ Đáp án A
HÓA HỌC LỚP 12
